OXOÀCIDS
- Els oxoàcids són compostos ternaris formats per la combinació d'hidrogen (H), oxigen (O) i un tercer element (X). La fórmula general d'un oxoàcid és HaXOb.
- El tercer element (X) s'anomena l'àtom central, i pot ser:
- Normalment un no metall: un element dels grups 13, 14, 15, 16 o 17.
- Un element de transició que actui amb nombres d'oxidació elevats. Els més freqüents són Cr, Mn, W, ...
- En els oxoàcids l'hidrogen sempre actua amb nombre d'oxidació +1 i l'oxigen amb nombre d'oxidació -2.
- El nombre d'oxidació de l'atom central es pot determinar aplicant la regla que diu que la suma dels nombres d'oxidació de tots els àtoms en un compost ha de ser zero. Si anomenem x al nombre d'oxidació de l'àtom central:
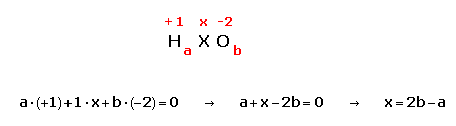
Per tant, el nombre d'oxidació de l'àtom central en un oxoàcid ve donat per l'expressió x = 2b-a, essent a el nombre d'àtoms d'hidrogen i b el nombre d'àtoms d'oxigen.
- Els oxoàcids tenen noms tradicionals admesos per la IUPAC, que són d'ús molt freqüent. Estudiarem en detall aquesta nomenclatura.
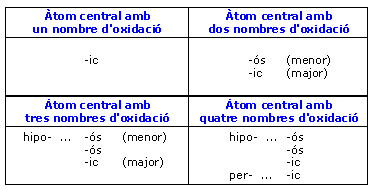
- El nom dels oxoàcids s'indica amb la paraula àcid seguida del nom de l'àtom central amb els prefixos (hipo-, per-) o els sufixos (-ós, -ic) que corresponguin, segons el nombre d'oxidació de l'àtom central.
- Quan l'àtom central és B,
Si, P
o As, per a cada nombre d'oxidació
hi ha dos oxoàcids. L'oxoàcid amb el menor contingut d'oxigen
s'anomena meta, i el que conté
un major contingut d'oxigen, orto.
En tots els casos, els oxoàcids orto tenen un àtom d'oxigen
i dos d'hidrogen més que els corresponents meta.
Els oxoàcids orto són més corrents que els meta. Si no es posa cap prefix, es sobreentén que es tracta de l'orto.
- En pràcticament tots els oxoàcids que considerarem hi ha només un àtom de l'element central. En el cas que n'hi hagi dos, cal afegir el prefix di davant del nom de l'àtom central.
Grup 13
| B | +3 |
HBO2 |
àcid metabòric |
| H3BO3 | àcid ortobòric o bòric |
Grup 14
| C | +4 |
H2CO3 |
àcid carbònic |
| Si | +4 | H2SiO3 | àcid metasilícic |
| H4SiO4 | àcid ortosilícic o silícic |
Grup 15
| N | +3 | HNO2 | àcid nitrós |
| +5 | HNO3 | àcid nítric | |
| P | +3 | HPO2 | àcid metafosforós |
| H3PO3 | àcid ortofosforós o fosforós | ||
| +5 | HPO3 | àcid metafosfòric | |
| H3PO4 | àcid ortofosfòric o fosfòric | ||
| As | +3 | HAsO2 | àcid metaarseniós |
| H3AsO3 | àcid ortoarseniós o arseniós | ||
| +5 | HAsO3 | àcid metaarsènic | |
| H3AsO4 | àcid ortoarsènic o arsènic |
Grup 16
| S | +4 | H2SO3 | àcid sulfurós |
| +6 | H2SO4 | àcid sulfúric | |
| Se | +4 | H2SeO3 | àcid seleniós |
| +6 | H2SeO4 | àcid selènic |
Grup 17
| Cl | +1 | HClO | àcid hipoclorós |
| +3 | HClO2 | àcid clorós | |
| +5 | HClO3 | àcid clòric | |
| +7 | HClO4 | àcid perclòric | |
| Br | +1 | HBrO | àcid hipobromós |
| +3 | HBrO2 | àcid bromós | |
| +5 | HBrO3 | àcid bròmic | |
| +7 | HBrO4 | àcid perbròmic | |
| I | +1 | HIO | àcid hipoiodós |
| +3 | HIO2 | àcid iodós | |
| +5 | HIO3 | àcid iòdic | |
| +7 | HIO4 | àcid periòdic |
Oxoàcids amb més d'un àtom de l'element central
|
H4P2O7 |
àcid difosfòric |
| H2S2O7 | àcid disulfúric |
Oxoàcids del metalls de transició
|
H2CrO4 |
àcid cròmic |
| H2Cr2O7 | àcid dicròmic |
| H2MnO4 | àcid mangànic |
| HMnO4 | àcid permangànic |
| Nomenclatura funcional |
|
| Nomenclatura sistemàtica |
|
- La següent taula mostra alguns exemples:
|
Fórmula
|
Funcional
|
Sistemàtica
|
| HBO2 | àcid dioxobòric (III) | dioxoborat (III) d'hidrogen |
| H2CO3 | àcid trioxocarbònic | trioxocarbonat d'hidrogen |
| HNO3 | àcid trioxonítric (V) | trioxonitrat (V) d'hidrogen |
| H3PO4 | àcid tetraoxofosfòric (V) | tetraoxofosfat (V) d'hidrogen |
| H2SO4 | àcid tetraoxosulfúric (VI) | tetraoxosulfat (VI) d'hidrogen |
| HClO | àcid monoxoclòric (I) | monoxoclorat (I) d'hidrogen |
| HIO4 | àcid tetraoxoiòdic (VII) | tetraoxoiodat (VII) d'hidrogen |
| HMnO4 | àcid tetraoxomangànic (VII) | tetraoxomanganat (VII) d'hidrogen |
| H2Cr2O7 | àcid heptaoxodicròmic (VI) | heptaoxodicromat (VI) d'hidrogen |
- A efectes de formulació i nomenclatura, els tioàcids poden considerar-se oxoàcids on un àtom d'oxigen (O) ha estat substituït per un àtom de sofre (S).
| Nomenclatures tradicional, funcional i sistemàtica |
|
- Estudiarem només dos tioàcids:
| Oxoàcid | H2SO3 | H2SO4 |
| Tioàcid | H2S2O2 | H2S2O3 |
| Tradicional | àcid tiosulfurós | àcid tiosulfúric |
| Funcional | àcid dioxotiosulfúric (IV) | àcid trioxotiosulfúric (VI) |
| Sistemàtica | dioxotiosulfat (IV) d'hidrogen | dioxotiosulfat (VI) d'hidrogen |